Методы познания веществ и химических реакций
Оглавление
- Определение характера среды водных растворов веществ. Индикаторы
- Качественные реакции на неорганические вещества и ионы. Катионы
- Качественные реакции на анионы
- Идентификация органических соединений
- Проба на окрашивание пламени
- Шпаргалка
- Задания для самопроверки
Определение характера среды водных растворов веществ. Индикаторы
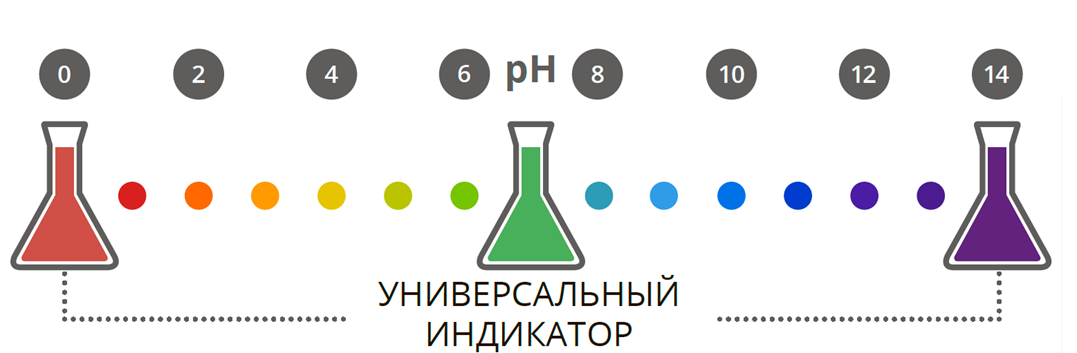
В школьном курсе химии знакомство учащихся с индикаторами сводится в основном к лакмусу, метиловому оранжевому и фенолфталеину. Между тем химических индикаторов гораздо больше.
Приведем одно из наиболее общих определений индикатора: индикатор — это вещество, указывающее на состояние системы или на момент, в который система достигает требуемого равновесия. Для химиков важно, что индикатор своим состоянием показывает наличие достаточной концентрации определяемого вещества.
Чтобы индикатором можно было пользоваться на практике, изменение его состояния должно легко фиксироваться. Как правило, индикаторы под воздействием определяемого вещества меняют цвет, иногда — агрегатное состояние, флуоресцируют. Существуют индикаторы кислотно-основные (рН-индикаторы), окислительно-восстановительные (редокс-индикаторы), а также индикаторы на какое-либо определенное вещество или группу веществ. Основной принцип работы индикатора — взаимодействие с определяемым веществом с образованием формы, имеющей другие свойства, чем исходная.
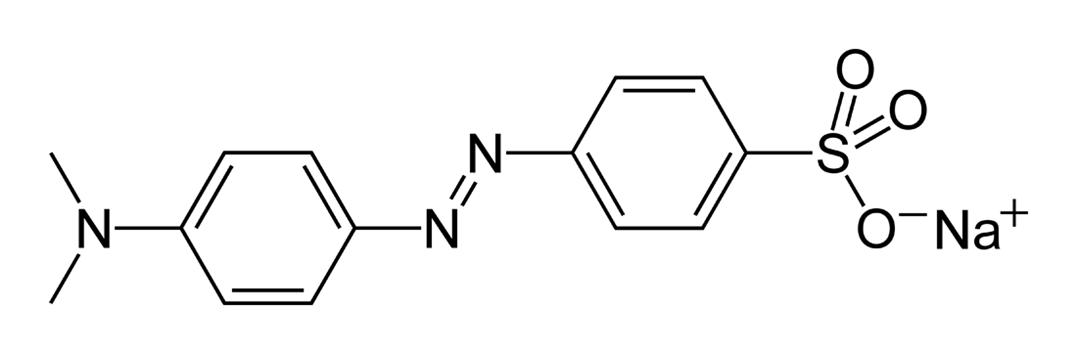
В частности, pH-индикаторы представляют собой органические кислоты, основания или соли. Например, метиловый оранжевый — это органическое основание Льюиса желтого цвета, которое под действием кислоты (ионов Н+) превращается в соль красного цвета:
Реакция обратима: при добавлении щелочи к соли ионы Н+, связанные с атомами азота, будут взаимодействовать с ионами ОН— с образованием молекул воды и равновесие сдвинется в сторону основания. Поэтому при подщелачивании метиловый оранжевый снова станет желтым.
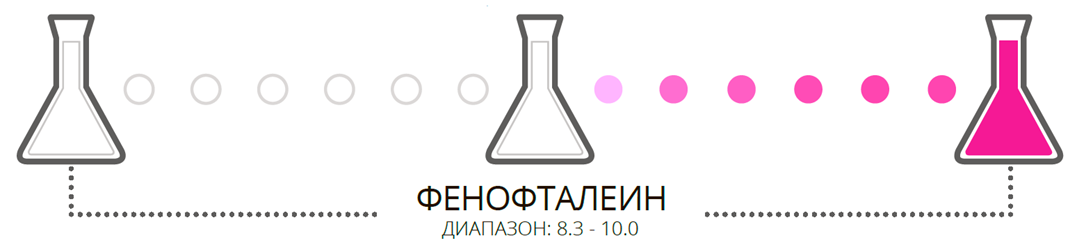
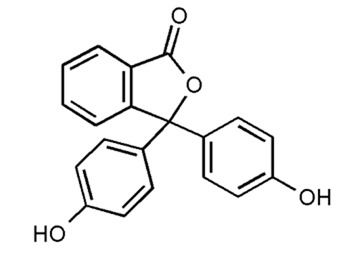
Принцип действия фенолфталеина примерно такой же. Фенолфталеин — бесцветный лактон, образующий под действием основания малиновый анион кислоты:
Ниже приведены различные индикаторы, однако для школьного курса химии достаточно знать такие индикаторы как лакмус, метиловый оранжевый и фенофталеин:
Качественные реакции на неорганические вещества и ионы. Катионы
Качественный анализ – раздел аналитической химии, посвященный установлению качественного состава веществ, то есть обнаружению элементов и образуемых ими ионов, входящих в состав и простых, и сложных веществ. Делают это с помощью химических реакций, характерных для данного катиона или аниона, позволяющих обнаружить их как в индивидуальных веществах, так и в смесях.
Задачей качественного анализа является изучение методов, с помощью которых устанавливают, какие химические элементы входят в состав анализируемой пробы.
Химические методы анализа основаны на применении характерных химических реакций для открытия составных частей вещества. Применяемые для этих реакции вещества называются реактивами.
Согласно теории электролитической диссоциации реакции протекают между ионами электролитов, образующимися в водных растворах. Происходящие при этом химические процессы называются аналитическими реакциями.
Они сопровождаются характерными внешними признаками, легко воспринимаемыми нашими органами чувств:
· выделение газа
· изменение окраски раствора
· выпадение осадка
· растворение осадка
· образование кристаллов характерной формы
В первых четырех случаях за протеканием реакции наблюдают визуально, кристаллы рассматривают под микроскопом
Для получения правильных результатов необходимы реакции, выполнению которых не мешают другие присутствующие ионы. Для этого нужны специфические (взаимодействующие только с определяемым ионом) или хотя бы селективные (избирательные) реагенты.
Примером реакции с участием специфического реагента является выделение газообразного NH3 при действии сильных оснований (KOH или NaOH) на вещество, содержащее ион NH4+. Ни один катион не помешает обнаружению иона NH4+, потому что только он реагирует со щелочами с выделением NH3.
Диметилглиоксим (реагент Чугаева) служит примером селективного реагента: в щелочной среде он реагирует с ионами Ni2+, Co2+, Fe2+, а в кислой – только с ионами Pd2+.
К сожалению, селективных, тем более специфических реагентов очень мало, поэтому при анализе сложной смеси приходится прибегать к маскированию мешающих ионов, переводя их в реакционно инертную форму, или, чаще, к разделению смеси катионов или анионов на составные части, называемые аналитическими группами. Делают это с помощью специальных (групповых) реагентов, которые с рядом ионов, реагируя в одних и тех же условиях, образуют соединения с близкими свойствами – малорастворимые осадки или устойчивые растворимые комплексы. Это и позволяет разделить сложную смесь на более простые составные части.
Существует несколько схeм деления катионов на аналитические группы с помощью групповых реагентов. Одна из них основана на использовании различий в растворимости хлоридов, сульфатов и гидроксидов. Действуя на смесь катионов в строго определенном порядке растворами HCl, H2SO4, NH3 и NaOH (групповые реагенты), можно разделить содержащиеся в смеси катионы на 6 аналитических групп. Эту схему называют кислотно-щелочной по именам используемых в ней групповых реагентов.
Смотрите качественные реакции на катионы в таблице ниже:
Качественные реакции на анионы
Анионы не имеют общеустановленного разделения на группы, число которых значительно варьирует в разных схемах анализа. Обычно анионы классифицируют по признаку растворимости солей и по признаку окислительной-восстановительной активности.
Групповые реагенты в анализе анионов служат только для их обнаружения (в отличие от катионов, где такие реактивы служат и для разделения).
Смотрите качественные реакции на анионы в таблице ниже:
Идентификация органических соединений
Органическая химия, как вы знаете, это химия углеводородов и их производных.
В состав углеводородов входят элементы углерод и водород. В составе производных углеводородов кроме углерода и водорода могут содержаться кислород, азот, сера, галогены и другие элементы.
Для обнаружения в составе органического соединения тех или иных элементов требуется разрушение его молекулы и перевод составляющих его элементов в простейшие соединения.
Анализ элементного состава может проводиться как качественное определение элементов, входящих в состав органических соединений (С, Н, О, N, S, Cl), так и количественное, показывающее процентное содержание каждого элемента в анализируемом органическом соединении.
Присутствие тех или иных элементов в органическом соединении может быть обнаружено различными методами качественного анализа.
Галогены, например, можно обнаружить качественной пробой Бейльштейна по изменению окраски пламени при внесении медной проволоки с пробой анализируемого вещества в пламя газовой горелки, что объясняется образованием летучих при высокой температуре галогенидов меди. Эта проба чувствительна даже на присутствие следов галогена в органических соединениях.
Проба на окрашивание пламени
Ряд элементов окрашивает пламя в характерный цвет, если под воздействием тепла в пламени появляются отдельные атомы этих элементов. У некоторых элементов атомы отделяются уже при первом погружении в пламя, у иных для этого требуется обработка кислотой. Если в определителе нет других специальных указаний, то обломок минерала надо смочить каплей разбавленной соляной кислоты, которая наносится с помощью стеклянной палочки или пипетки, а затем прокалить.
При совершении электроном квантового скачка с одной разрешенной орбитали на другую атом испускает свет. А поскольку энергетические уровни атомов двух элементов различны, свет, испускаемый атомом одного элемента, будет отличаться от света, испускаемого атомом другого. Это положение лежит в основе науки, которую мы называем спектроскопией.
На этом же положении (что атомы разных элементов испускают свет разной длины волны) основана проба на окрашивание пламени в химии. При нагревании в пламени газовой горелки раствора, содержащего ионы одного из щелочных металлов (то есть одного из элементов первой колонки периодической системы Менделеева), пламя окрасится в определенный цвет в зависимости от того, какой металл присутствует в растворе. К примеру, ярко-желтый цвет пламени выдает присутствие натрия, фиолетовый — калия, а карминно-красный — лития. Происходит это окрашивание пламени так: столкновение с горячими газами пламени переводит электроны в возбужденное состояние, из которого они возвращаются в исходное, одновременно испуская свет характерной длины волны.
Это свойство атомов объясняет, почему лес, прибитый к океанскому берегу, так высоко ценится для топки каминов. Долгое время находясь в море, бревна адсорбируют большое количество разных веществ, и при горении бревен эти вещества окрашивают пламя во множество разных цветов.
Шпаргалка
Справочный материал для прохождения тестирования:






























![clip_image003[1] clip_image003[1]](/wp-content/uploads/2017/04/clip_image0031_thumb-1.png)